 医薬品規制当局が中国企業による最初の「中国製」PD-1医薬品申請を承認
医薬品規制当局が中国企業による最初の「中国製」PD-1医薬品申請を承認(Yicai Global) 12月15日-中国の食品医薬品局は、腫瘍免疫薬であるPD-1として知られる「プログラムされた細胞死タンパク質1」の放出を求める中国の製薬会社の申請を承認しました。江蘇省に本拠を置くInnovent Biologics Inc. によって開発され、この種の最初の「中国製」薬です。
Innoventは、中国の食品および医薬品の医薬品評価のためにセンターに申請書を提出しました。12月13日、オンラインメディアアウトレットCaixin.comは昨日述べた。アプリケーションで指定されているように、この薬は、リンパ球と呼ばれる細胞で始まる癌の一種であるホジキンリンパ腫の治療に使用されます。成功すれば、他の種類の腫瘍を治療するために拡張されます。
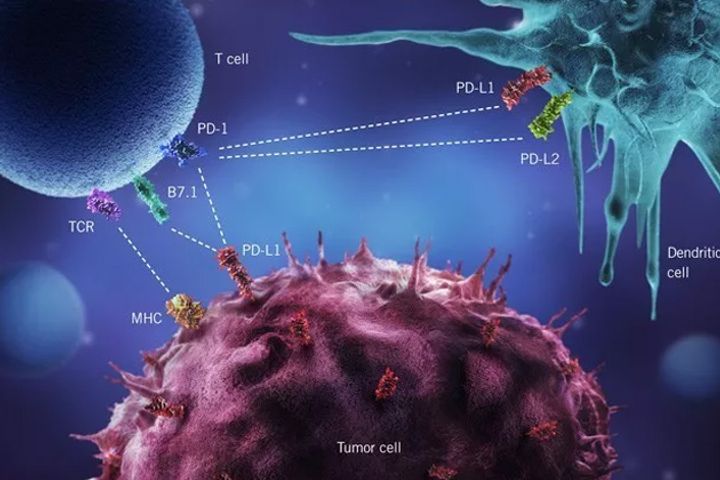
PD-1は、患者自身の免疫システムを通じて腫瘍を破壊し、自己寛容を促進する薬を指します。それは多数の種類の腫瘍を扱うことは利用できます。他の国、特に末期がん患者に広く使用されています。
現在、中国でこの薬の臨床試験を実施している製薬企業は9社あります。約10の企業もその臨床試験に申請しています。
外国企業の中で、米国を拠点とするブリストルマイヤーズスクイブ社 [NYSE:BMY] は先月、承認を待っている中国の医薬品規制当局にPD-1の公開申請を提出しました。